Bateria osmótica
Sempre houve muito interesse em extrair eletricidade da diferença de salinidade entre rios e oceanos, uma fonte de energia limpa, renovável e virtualmente quase inesgotável.
Quando dois corpos de água com salinidades diferentes se encontram, as moléculas de sal fluem naturalmente de uma concentração mais alta para uma concentração mais baixa. Isso não é muito diferente do que acontece dentro de uma bateria recarregável comum, com a diferença de que as baterias mais vendidas atualmente são de íons de lítio, enquanto a bateria na foz dos rios seria uma bateria de íons de sódio - o sal marinho é basicamente cloreto de sódio.
Mas fabricar essas baterias osmóticas, ou baterias naturais de íons de sódio, tem-se mostrado um desafio difícil de vencer.
Agora, Zhijiang Xie e colegas da Universidade Agrícola de Anhui, na China, trouxeram uma nova esperança para esta área criando um protótipo de bateria osmótica que alcançou uma densidade de energia nada menos do que 2,34 vezes superior às já demonstradas, trazendo um novo alento de que essa tecnologia possa se tornar comercialmente viável.
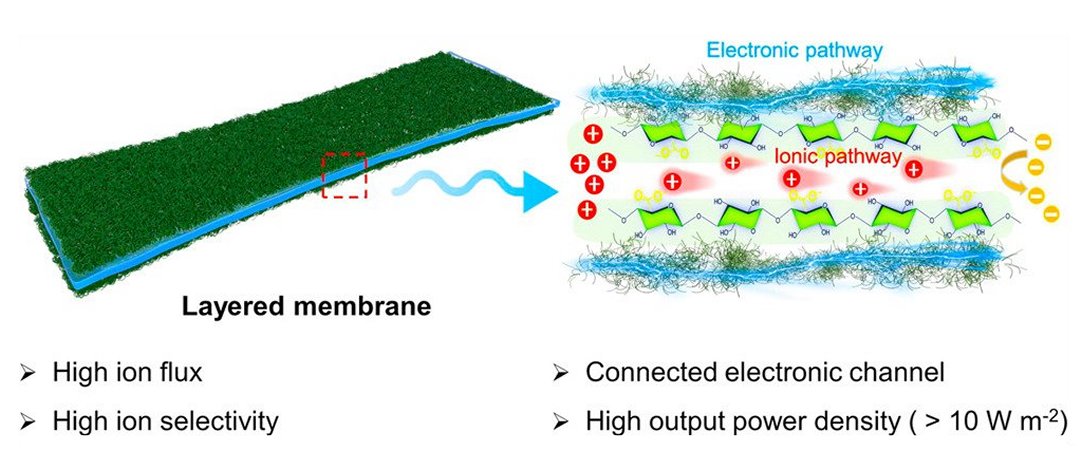
A estrutura isotrópica, separando as cargas eletrônicas e iônicas, foi crucial para o elevado rendimento alcançado.
[Imagem: Zhijiang Xie et al. - 10.1021/acsenergylett.4c00320]
Membrana de eletrodiálise reversa
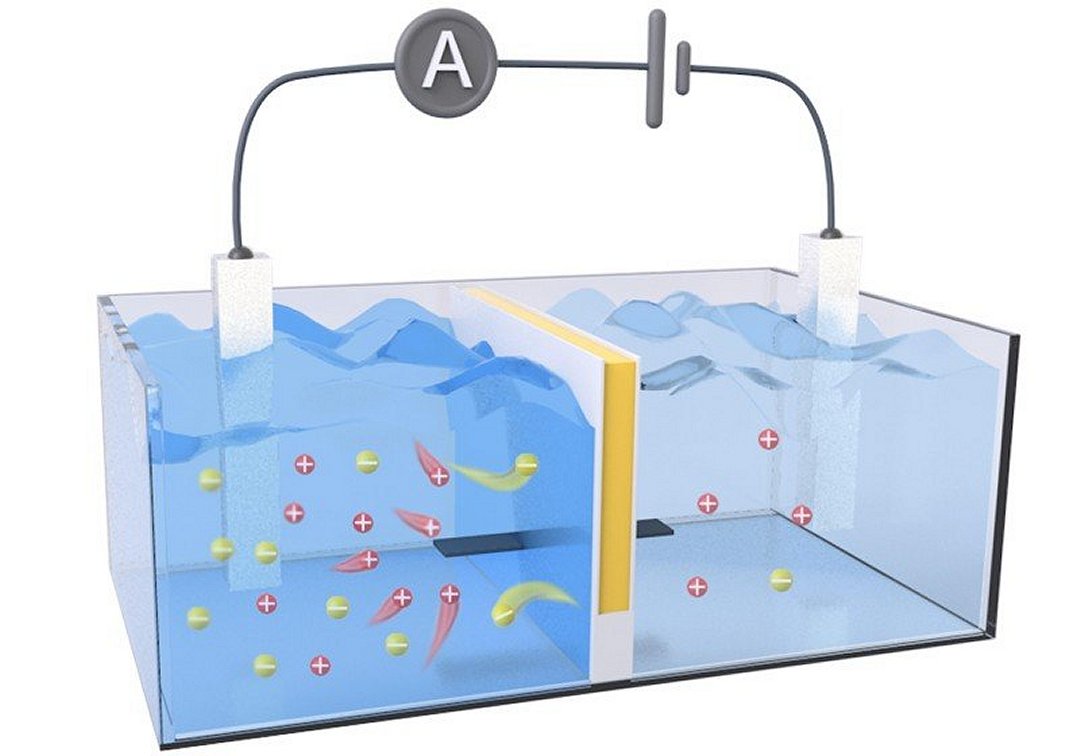
O elemento chave de uma bateria osmótica é a membrana que guia os íons de sódio, coletando energia osmótica dos gradientes de sal entre a água do mar e a água doce do rio que deságua, e a converte em eletricidade.
Um método para fazer isto consiste em um conjunto de membranas de eletrodiálise reversa (MER) que funcionam como uma bateria de sal, gerando eletricidade a partir das diferenças de pressão causadas pelo gradiente salino. Para equilibrar esse gradiente, íons carregados positivamente da água do mar, como o sódio, fluem através das membranas rumo à água doce, aumentando a pressão na membrana.
Para aumentar ainda mais seu poder de colheita de energia, a membrana também precisa manter uma baixa resistência elétrica interna, permitindo que os elétrons fluam facilmente na direção oposta à dos íons. Xie e seus colegas criaram então uma membrana que faz justamente isto, melhorando tanto o fluxo de íons quanto a eficiência do transporte de elétrons, o que aumenta a quantidade de eletricidade capturada da energia osmótica.
A nova membrana semipermeável também foi fabricada usando apenas materiais ambientalmente benignos, o que é essencial para sua utilização diretamente em estuários, onde a foz dos rios é larga e mansa o suficiente para a exploração comercial do conceito.
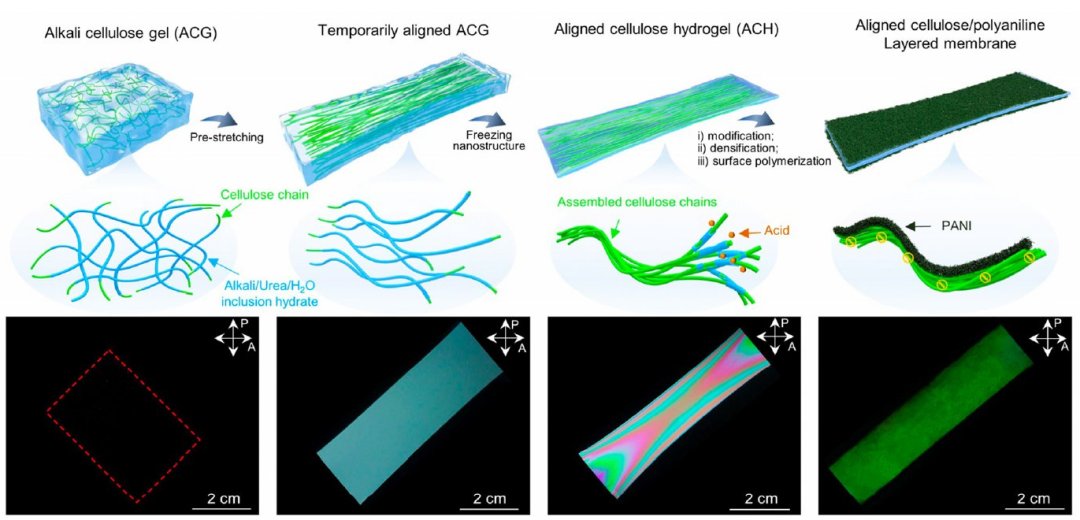
Todos os materiais utilizados são ambientalmente benignos.
[Imagem: Zhijiang Xie et al. - 10.1021/acsenergylett.4c00320]
Protótipo da bateria osmótica
O protótipo de membrana MER (membrana de eletrodiálise reversa) conta com canais separados para transportar os íons e os elétrons, o que foi conseguido ensanduichando um hidrogel de celulose (com carga negativa, para transporte dos íons) entre camadas de um polímero orgânico eletricamente condutor chamado polianilina (com carga negativa, para transporte dos elétrons).
Os testes iniciais confirmaram a teoria de que canais de transporte desacoplados resultam em maior condutividade iônica e menor resistividade eletrônica em comparação com membranas homogêneas feitas dos mesmos materiais. Em um tanque de água que simula um ambiente de estuário, o protótipo alcançou uma densidade de potência de saída 2,34 vezes maior do que uma membrana MER comercial e manteve o desempenho praticamente inalterado durante os 16 dias de operação ininterrupta a que os pesquisadores submeteram a bateria.
Em um teste final, apenas para demonstração em escala de laboratório, a equipe criou um conjunto de baterias de íons de sódio usando 20 de suas membranas MER - o empilhamento de 20 camadas permitiu atingir uma tensão de 2,2 volts. O conjunto atingiu uma densidade de potência de saída de 11,7 W m-2 e manteve um desempenho de saída de 10,9 W m-2 após 16 dias de operação.